Атопический дерматит (АтД)
— хроническое воспалительное заболевание кожи, в развитии которого принимают участие как внешние триггеры, среди которых могут быть различные вещества белковой природы, приводящие к сенсибилизации организма, так и внутренние факторы, такие как несостоятельность кожного барьера с нарушением его защитных свойств вследствие развития дисбаланса врожденного иммунитета [1]. Предрасполагающие к АтД внутренние факторы наследуются гетерогенно и реализуются под воздействием условий внешней среды. Наличие в генотипе даже нескольких значимых для формирования АтД мутаций не всегда приводит к появлению кожного симптома [2]. Триггерами АтД могут выступать как аллергены, так и неспецифические факторы — экологические, физические; в последнее время все чаще обращают внимание на возможность участия в поддержании обострения болезни психоэмоционального стресса. Известно, что АтД является одним из 8 психосоматических заболеваний [3].
Дизрегуляция механизмов формирования кожного барьера способствует нарушению сальности кожи и потере воды, несостоятельность защитных свойств рогового слоя кожи — трансэпидермальной сенсибилизации организма к бытовым и пыльцевым аллергенам, а формирующийся очаг воспаления — колонизации кожи условно-патогенной флорой. В 9 из 10 случаев у пациентов с АтД с пораженных кожных покровов высевают штаммы Staphylococcus aureus, имеющего самостоятельное патогенетическое значение при этом заболевании.Известно, что энтеротоксины стафилококков, являясь суперантигенами, способны расширять спектр сенсибилизации организма и поддерживать местный воспалительный процесс [4]. В последних исследованиях обнаружена прямая связь между степенью колонизации кожных покровов S. аureus и прогрессированием АтД [5–7].
Здоровую кожу ребенка можно рассматривать как многоуровневую систему взаимосвязанных физиологических и иммунологических барьеров, удерживающих влагу и препятствующих проникновению в кожу чужеродных веществ и патогенных микроорганизмов [7].
Повреждение рогового слоя возможно вследствие дефицита структурных белков — филаггрина, инволюкрина, лорикрина и липидов. Снижение защитной функции кожи, связанное с дисбалансом клаудинов — плотно примыкающих друг к другу белков, находящихся на обратной стороне кератиноцитов, усугубляет трансэпидермальную потерю воды, приводя к выраженной сухости кожных покровов. Указанные белки образуют в эпидермисе второй физиологический барьер. Несостоятельность кожного барьера из-за дефицита структурных белков способствует немедленной ответной реакции врожденного и приобретенного иммунитета, сопровождающейся экспрессией на мембранах кератиноцитов антигенпрезентирующих клеток Toll-подобных рецепторов (TLR). Стимуляция TLR с выбросом антимикробных пептидов и увеличением белковых контактов играет важную роль как фактор, препятствующий дальнейшему проникновению в кожу чужеродных агентов [8].
Дисфункция кожного барьера вызывает развитие Th2-воспаления [9]. Переизбыток Th2-цитокинов в коже подавляет экспрессию генов основного антимикробного пептида — бета-дефенсина-3 (hBD-3) в кератиноцитах [10]. Выброс кератиноцитами при АтД противомикробных пептидов оказывается недостаточным для контроля инфицирования кожи S. аureus и вирусной репликации [11]. Возникает порочный круг: воспалительный процесс способствует инфицированию кожи, а S. аureus еще больше нарушает барьерные функции кожи, усугубляя течение АтД. Колонизация кожи бактерией у пациентов с АтД достигает высоких значений: по данным ряда авторов, 55–90 против 5% у здоровых людей [12, 13]
S. аureus способен ухудшать состояние кожного барьера вследствие выброса большого количества сериновых протеаз. Колонизация кожи бактерией может усиливать зуд; в периферической крови у больных с АтД обнаруживают специфические IgE к токсинам стафилококка, способным выступать в качестве суперантигенов [14]. Стафилококковый энтеротоксин В, связываясь с TNF-рецептором моноцитов, ингибирует иммуносупрессивную активность Treg-клеток и стимулирует пролиферацию С-волокон с последующим усилением нейрогенного зуда в эксперименте на крысах, а у человека на здоровой коже вызывает экзематозные поражения [15].
Наравне с гипотезой, указывающей в качестве главной причины дебюта АтД нарушение барьерной функции кожи при наличии генетических мутаций ее структурных белков [16], существуют достаточно убедительные доводы в пользу участия в развитии данного патологического процесса переключения ответа иммунной системы на Th2-путь, сопровождающийся подавлением дифференцировки и апоптоза кератиноцитов, что ведет к еще большей несостоятельности защитных свойств кожи.
Наряду с убедительными доказательствами влияния мутации гена филаггрина на течение АтД интересны факты развития достаточно тяжелых форм АтД при отсутствии данной мутации [17] и в то же время — обнаружения ее у людей без кожных заболеваний [18]. Известно, что большинство детей, имеющих подобные мутации, «перерастают» АтД [19]. Вдобавок к этому в отличие от картины врожденных генетических болезней кожи при АтД имеются участки как пораженной, так и непораженной кожи. При этом на измененных и неизмененных участках кожи выявляется широкий спектр различных аномалий других структурных белков (лорикрин, инволюкрин, клаудины и т. д.) [20].
Необходимо также подчеркнуть, что в основе поражения кожи при АтД лежит активация иммунной системы. Хроническое течение АтД сопровождается усиленной (примерно в 10 раз большей, чем в норме) инфильтрацией кожи Т-лимфоцитами и дендритными клетками [21], увеличением продукции цитокинов и хемокинов в очагах воспаления, гиперплазией эпидермиса с крайне высоким количеством структурных белков в стадиях терминальной дифференцировки. Все это — открытые вопросы, что диктует необходимость дальнейшего поиска причин дебюта и прогрессирования АтД.
АтД — достаточно распространенное заболевание [22]. Сегодня оно привлекает внимание многих исследователей из разных стран, которые проводят большое число фундаментальных и клинических исследований.В последние годы появились новые данные о эпигенетике и иммунопатогенезе заболевания; параллельно
разрабатываются инновационные методы лечения. Над Проблемой АтД работают ученые всего мира, которые суммируют накопленные знания и продвигают свои идеи. Включение любого пациента с АтД в исследование, в котором изучаются особенности течения болезни (будь то научные разработки по генетике, патогенезу или современным программам лечения), требует четкой постановки диагноза, одинаковой для всех больных любой страны мира.
На сегодня не разработано рутинной лабораторной диагностики этого состояния. Врачи и ученые-исследователи ориентируются на клинические критерии, которые выделены с целью единообразной постановки диагноза в разных научных и клинических центрах. Чаще всего (в 41,0% случаев) используются диагностические критерии Hanifin и Rajka; английские критерии применяют в 9,0% случаев, японские — в 4,2% и американские — в 3,8% [23].
Критерии Hanifin и Rajka делятся на основные и вспомогательные, их необходимо учитывать при постановке диагноза АтД [24]. Многие исследователи и врачи обращают внимание на то, что некоторые вспомогательные критерии могут быть перенесены в основные, так как отсутствие их в перечне основных критериев нередко ведет к путанице и снижению качества лечения больных. Самые обсуждаемые моменты — оценка роли сенсибилизации в развитии АтД и наличия выраженной сухости кожных покровов.
Действительно, относительно недавние открытия и исследования в области иммунологии четко установили связь поражения кожи, свойственное АтД, с дисбалансом иммунной системы, сопровождающимся выработкой аллерген-специфических IgE. На протяжении многих лет обсуждается влияние сенсибилизации к различным аллергенам на возникновение и прогрессирование этого заболевания [25]. В то же время установлено, что наличие у больного с АтД выраженной чувствительности к пищевым или бытовым аллергенам, скорее, позволяет поставить диагноз атопического синдрома, а не АтД. В настоящее время из определения заболевания выведено название «аллергическое воспалительное кожное заболевание», так как такая позиция приводит к обязательному поиску у больных внешнего триггера воспаления с назначением необоснованных ограничительных режимов [26]. По данным последних исследований, сенсибилизация при этом состоянии подтверждается менее чем в 50% случаев, лишь у 30–40% пациентов отмечают проявления пищевой аллергии, часто — в случаях среднетяжелого и тяжелого течения АтД с развитием в дальнейшем толерантности ко многим пищевым белкам у детей старшего возраста [27]. Подчас в дополнение к обязательным 4 основным критериям диагностики АтД (зуд; типичная морфология и локализация поражения кожи; хроническое, непрерывно рецидивирующее течение и наследственная отягощенность) добавляют критерий наличия у больного тотальной сухости кожных покровов [28]. Действительно, прогрессирующее течение АтД сопровождается этим симптомом; в клинических рекомендациях всех стран есть указания на необходимость использования в базисной терапии увлажняющих наружных средств, способных продлевать ремиссию.
Как уже говорилось, критерии Hanifin и Rajka наиболее часто используются в клинических исследованиях. В период с 2007 по 2016 г. в педиатрической и взрослой популяции они применяются в большинстве стран [23]. Согласно им, диагноз АтД подтверждается при наличии 3 из 4 основных и 3 из 19 второстепенных диагностических критериев [29].
Сейчас не подвергается сомнению необходимость контроля одного из вспомогательных критериев АтД — сухости кожных покровов. Восстановление кожного барьера позволяет снизить риск очередного обострения заболевания после успешного наружного противовоспалительного лечения. Фармацевтический рынок предлагает различные косметические наружные средства, рекомендованные для контроля состояния кожи при АтД.
В настоящее время на рынке появился новый крем с 7% содержанием молекулы эктоина — Перфэктоин®. Он сочетается с любыми препаратами и может применяться в комплексной терапии при АтД, экземе, нейродермите, псориазе, контактном дерматите, радиационном дерматите, ретиноидном дерматите, хейлите, сухости кожи. Его можно использовать при проактивной терапии АтД благодаря его способности стабилизировать и защищать кожный барьер.
Многочисленные исследования подтвердили эффективность и безопасность применения эктоина при дерматозах. Кроме того, в креме отсутствуют потенциально вредные составляющие — консерванты, красители, поверхностно-активные вещества [30].
Основным компонентом крема является эктоин в концентрации 7% — уникальная молекула природного происхождения. Эктоин — открытие шведских ученых, уникальное вещество, вырабатываемое особыми микроорганизмами для защиты от неблагоприятных факторов окружающей среды.
Эктоин образует прочные связи с молекулами воды, формируя пленку на поверхности кожи — эктоин-гидрокомплекс, который:
- восстанавливает барьерную функцию кожи;
- удерживает влагу;
- препятствует воздействию раздражающих факторов и аллергенов;
- снижает воспаление и уменьшает зуд.

В состав крема Перфэктоин® входит липооптимумкомплекс, который восстанавливает оптимальный уровень увлажнения путем естественного восстановления водно-липидного баланса. Компонентами комплекса являются церамиды, сквалан, липиды натуральных масел (оливковое и масло ши), кардиоспермум халикакабский, триглицериды каприновой и каприловой кислот. Благодаря этим компонентам крем имеет нежную текстуру, даже небольшого его количества достаточно для нанесения на значительную площадь поверхности кожи.
Нами был проанализирован опыт применения у детей с АтД косметического средства Перфэктоин® для восстановления кожного барьера и контроля местного воспаления вокруг губ. Были обследованы 50 детей с легким и среднетяжелым течением АтД при среднем значении индекса SCORAD26 в период обострения основного заболевания. У 35 детей первых 3 лет жизни увлажняющее наружное средство использовали для восстановления кожного барьера на всей поверхности кожи, у 15 детей более старшего возраста с АтД и хейлитом (см. таблицу) Перфэктоин® наносили на кожу вокруг губ. Эффективность терапии через 2 нед нанесения крема оценивалась родителями пациентов субъективно по авторскому онлайн-опроснику с использованием платформы https://docs.google.com/forms.
Крем Перфэктоин® чаще всего использовали в период ремиссии АтД после эффективной противовоспалительной терапии. На фоне обострения АтД увлажняющее средство наносили вокруг губ при обострении хейлита и в составе комбинированного наружного лечения, включающего в себя применение наружных глюкокортикостероидов (ГКС) низкой и средней биологической активности (по Европейской классификации потенциальной активности местных ГКС, Miller & Munro). Эффективность увлажнения оценивали по 10-балльной системе: 0 — отсутствие эффекта, 10 — хороший эффект.
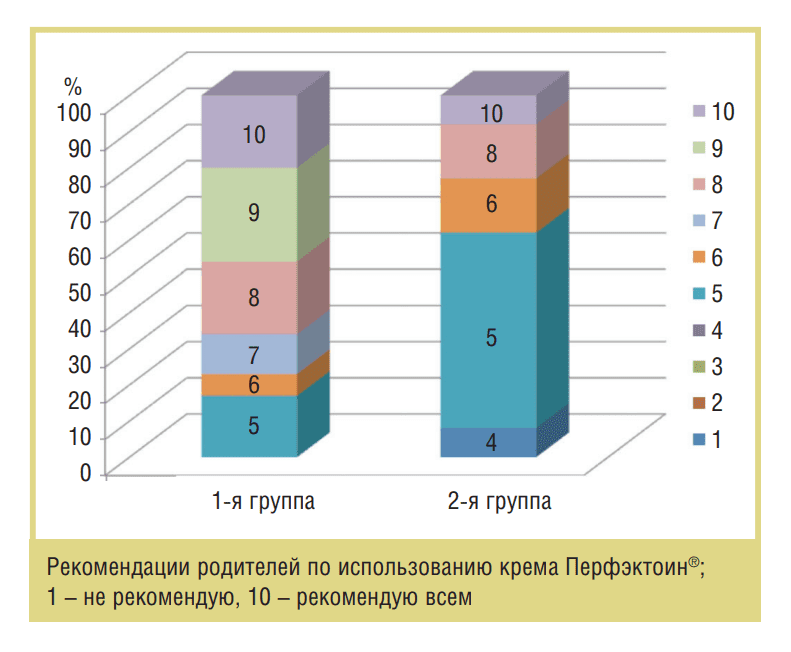
Родители детей с АтД отмечали хорошую переносимость крема Перфэктоин® при эффективном увлажнении кожи (см. рисунок) как в случае изолированного течения (1-я группа), так и при его сочетании с хейлитом (2-я группа) — соответственно 7,5 и 7,2 балла. Такой результат подтверждает уже имеющиеся данные о долгосрочном увлажняющем действии эктоина на кожу [30]. При использовании крема на фоне обострения основного заболевания в некоторых случаях отмечались неприятные ощущения в виде жжения и покраснения. В основном неприятные ощущения наблюдались лишь при 1-м нанесении препарата, в дальнейшем пациенты переносили его хорошо.
У 2 подростков и 2 пациентов 2-летнего возраста с хейлитом на фоне обострения АтД применение крема Перфэктоин® было прекращено из-за возникших неприятных ощущений со стороны кожных покровов вокруг губ. У остальных детей использование крема не сопровождалось жалобами и оценивалось как врачом, так и пациентами как хорошее (см. рисунок).
Таким образом, сухость кожных покровов, связанная с несостоятельностью кожного барьера и возникающей вследствие этого трансэпидермальной потерей воды наряду со снижением сальности кожи, наиболее часто сопровождает течение АтД и требует постоянного контроля с помощью увлажняющих наружных средств. Использование крема Перфэктоин® в комплексном лечении АтД позволяет поддержать нормальное физиологическое состояние кожи, способствуя восстановлению ее защитных свойств и баланса микробиоценоза.
* * *
Авторы заявляют об отсутствии конфликта интересов.
Информация о финансировании: финансовая поддержка отсутствовала.
